简介
该用户还未填写简介
擅长的技术栈
可提供的服务
暂无可提供的服务
质谱蛋白质组学可生成表征生物样品中肽段/蛋白质组分的复杂数据,各类机器学习是串联质谱肽段鉴定及数据分析全流程的核心计算方法。随着深度学习成为数据建模与解析的强力机器学习手段,蛋白质组学计算研究者利用海量公开数据集训练机器学习模型,用于预测肽段碎裂谱与液相色谱保留时间。ProteomicsML等资源为这类学习任务提供了详尽的演示教程,缩小了蛋白质组学与机器学习领域的隔阂。但现有深度学习教学材料普遍缺
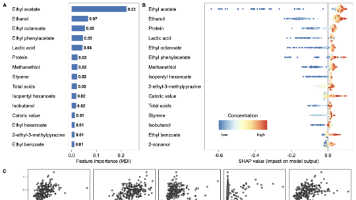
食品风味的感知与喜好受多种化合物互作及外部因素调控,难以解析和预测。本研究对250款啤酒开展全面化学检测与感官分析,训练机器学习模型以预测风味特征与消费者喜好。针对每款啤酒,检测200余项化学指标,由专业品鉴组完成定量描述性感官分析,并整合18万余条消费者评价,训练10种机器学习模型。表现最优的梯度提升算法模型显著优于传统统计预测方法,可通过化学图谱精准预测啤酒复杂风味与消费者喜好。模型解析筛选出
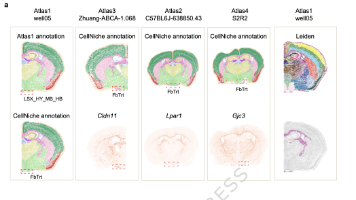
在图谱尺度解析细胞微环境仍面临核心挑战,原因是分子特征、空间语境与平台异质性3者高度耦合。本文提出可扩展的对比学习框架CellNiche,该框架以细胞为中心构建空间近邻子图,从空间组学数据中识别并表征细胞微环境。CellNiche融合空间共定位与分子共表达信号,学习微环境感知的嵌入表征。在来自多种平台、总计超1,000万个细胞的空间组学数据集中,扩展性实验证实:模型表征能力随训练数据量增加而提升,
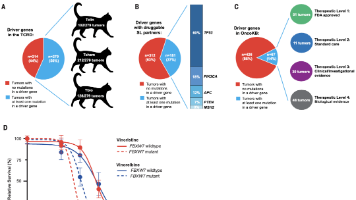
肿瘤是家猫发病和死亡的主要诱因。由于家猫肿瘤的突变谱尚未明确,本研究对13种肿瘤类型的493例家猫肿瘤-正常配对组织开展靶向测序,测序靶点聚焦于约1,000个人类癌症基因的猫同源基因。TP53是突变频率最高的基因,最常见的拷贝数变异为PTEN或FAS缺失、MYC扩增。本研究鉴定出31个驱动基因、突变特征、病毒序列及肿瘤易感生殖系变异,系统解析家猫肿瘤基因组特征。研究证实家猫肿瘤基因组与人类肿瘤基因
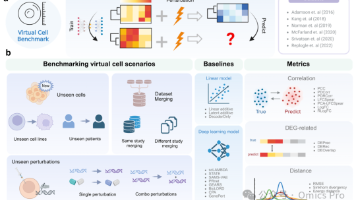
虚拟细胞模型旨在通过计算预测细胞对各类扰动的响应,已成为药物研发与精准医疗的前沿手段。但当前研究存在明显缺口:各类模型在标准基准测试中表现优异,但其预测结果在实际应用中的生物学意义尚不明确。这主要源于现有评估方案的缺陷——评估设置过度简化、流程不统一,无法反映真实生物系统的复杂性与变异性。本文提出1套标准化、模块化的虚拟细胞预测基准评测框架,在未见细胞背景、未见扰动类型、跨数据集泛化3类真实挑战性
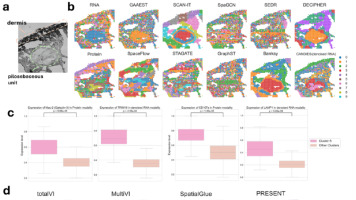
空间多组学数据可在保留细胞空间结构的同时,整合多种分子谱信息,是解析组织分子特征的强大工具。但不同模态间固有的数据质量与噪声水平差异,严重制约了数据的精准整合与分析。本文提出CANDIES框架,结合条件扩散模型与对比学习,实现空间多组学数据的高效去噪与整合。该框架凭借创新的模型与算法设计,既能提升空间多组学数据质量,又可生成统一、全面的联合表征,支撑多种下游生物学分析。
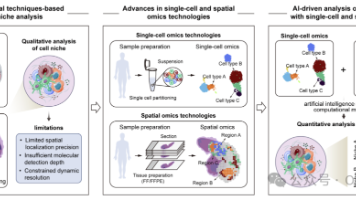
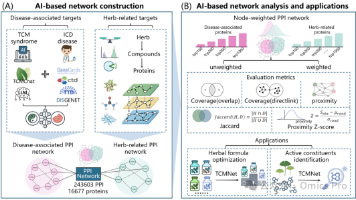
中医药的疗效以机体整体系统性调控为核心特征,通常通过协调组织微环境与多细胞互作实现。传统分子生物学方法难以精准解析组织水平的细胞组成、空间结构及微环境(细胞生态位cell niche),制约了对中医药作用机制的全面阐释。近年来,单细胞与空间组学技术快速发展,结合人工智能(AI)驱动的计算方法,实现了复杂组织内细胞生态位的系统解析,为中医药研究提供了新机遇。
思维导图经典方剂治疗PD效果排名(加权邻近度Z-score)加权vs未加权邻近度核心差异。
单细胞测序技术的快速发展催生了海量多组学数据,推动了大量整合工具的研发。尽管多组学整合极大推动了细胞研究,但目前仍缺乏针对这些工具的全面评测与应用指南。本研究针对多组学数据整合任务,开展「领域专用模型(DM)与基础模型(FM)」的基准评测,在整合准确性、生物标志物检测、轨迹推断、批次效应定量校正4个维度,对23种经超参数优化的方法进行评估。本研究填补了基础模型与领域专用模型在多组学整合任务中效能与

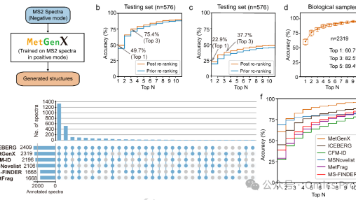
受参考质谱谱图数量有限的制约,代谢物注释(尤其是未知代谢物的发现)仍是基于质谱的非靶向代谢组学领域的核心难题。本研究开发了结构引导的编码器-解码器神经网络MetGenX,可直接从2级质谱(MS²)谱高效、可控地生成代谢物结构。MetGenX将「谱图到结构」的任务重构为「结构到结构」的生成问题,显著提升了生成准确率与化学空间覆盖度。独立测试中,该模型在1,388张美国国家标准与技术研究院(NIST)